Allgemeines
So entfernen Sie Rost an einer Gusspfanne
Es ist eine altbekannte Tatsache, dass jeder, der rastet, früher oder später auch anfängt zu rosten. Natürlich nicht wortwörtlich, das ist klar. Papier vergilbt, Holz wird morsch, Wein vergärt. Unsere hart antrainierte Kondition löst sich in Nichts auf (meistens leider viel zu schnell).
Also, nicht alles, was lange Zeit stillsteht, setzt tatsächlich Rost an. Doch Eisen, Eisen das rostet. Und unter geeigneten Umständen nicht zu knapp.

Grillpfanne demnächst wieder verfügbar
Die Tage sind gezählt - nicht mehr lange, bis die neue ROETH N° 1 Grillpfanne verfügbar ist.
Tragen Sie Ihre E-Mail im Verteiler ein und erhalten Sie einen Vorbesteller-Rabatt, sobald die neuen Grillpfannen erhältlich sind.
Vorbesteller-Rabatt sichernMittelalterliche Kanonengeschütze wirken erst so richtig schön mittelalterlich, wenn sie ein bisschen verfallen aussehen. Und von Rost überzogene Schubkarren eignen hervorragend als große Blumenkübel in einem wild wuchernden Garten. So einfach geht „Shabby Chic“.
Eine andere Sache ist es, wenn Rost Gegenstände befällt, die wir wirklich noch brauchen und eigentlich nicht so schnell ersetzen wollten. Meistens haben eher größere Unternehmen oder öffentliche Einrichtungen mit diesem Problem zu kämpfen und müssen sich immer wieder mit rostenden Stahlträgern und Eisenrohren in Gebäuden, Werkhallen und Brücken herumschlagen.
Hin und wieder trifft es jedoch auch uns. Zum Glück kann man etwas gegen Rost tun, wenn man ihn früh genug erkennt – doch dazu später mehr. Denn zuallererst müssen wir klären, ob unsere gusseiserne Pfanne Gefahr laufen könnte zu rosten.
Können Gusseisenpfannen rosten?

Der Aussage, dass Gusspfannen Freunde fürs Leben sind, ist nichts entgegenzusetzen. Unter normalen Umständen und bei ordnungsgemäßer Handhabung ist eine Eisenpfanne unzerstörbar und kann problemlos an die Urgroßenkel vermacht werden.
Bei der Frage nach Rostanfälligkeit ist das entscheidende Kriterium, ob die Gusspfanne mit einer Oberflächenbeschichtung überzogen ist. Unbeschichtete Pfannen können durchaus Rost ansetzen. Findet man auf Omas Dachboden also eine Eisenpfanne, die den Herd seit den guten alten Zeiten nicht mehr gesehen hat, darf man nicht überrascht sein, wenn sich an manchen Stellen Rost gebildet hat; selbst, wenn zuvor eine Patina eingebrannt worden ist.
Bei einer beschichteten Pfanne (dem üblichen Standard heutzutage) kann einem das nicht passieren – sofern die Oberflächenbeschichtung unbeschädigt ist. Warum ist das so?
Was ist Rost, und wie entsteht er?
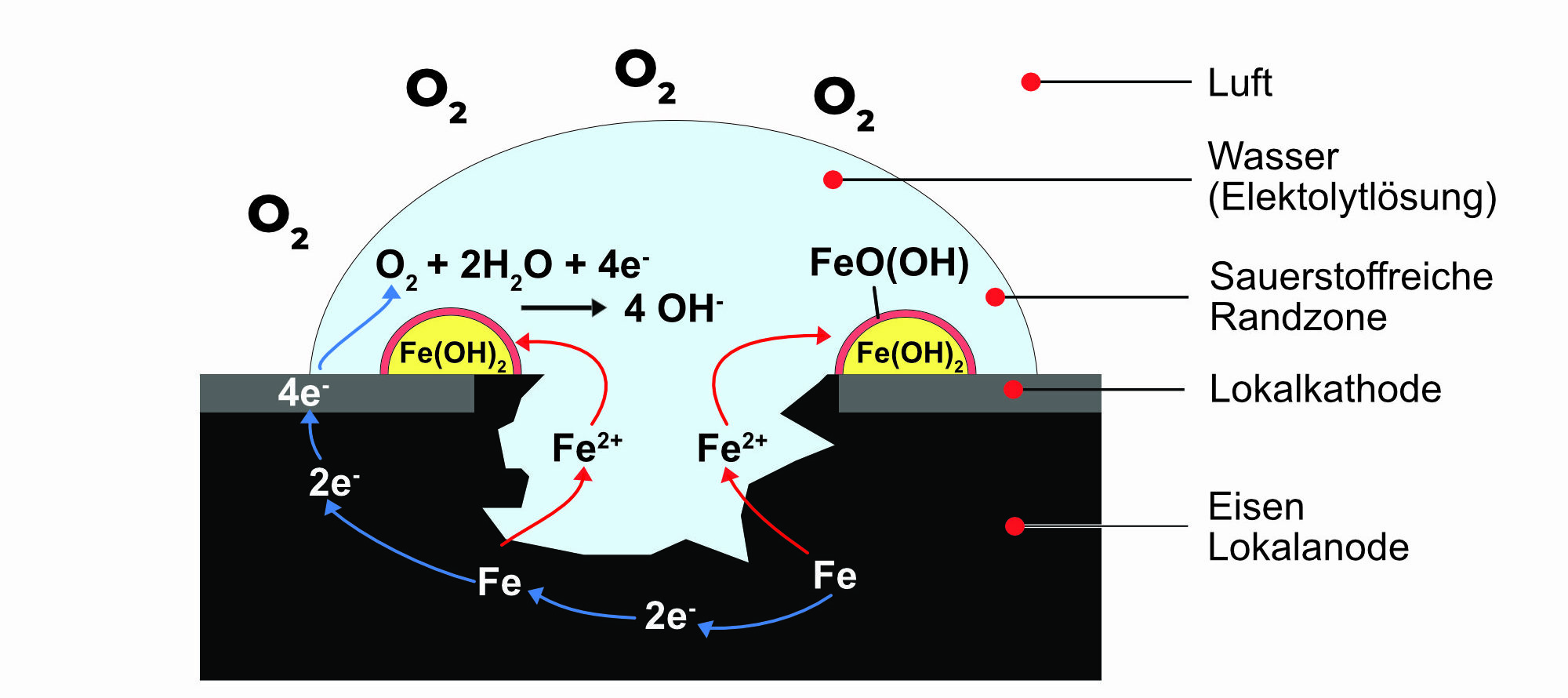
Rost entsteht, wenn sich Eisen und Sauerstoff durch Berührung mit Wasser miteinander verbinden. In Fachkreisen wird Rost daher auch als „Eisenoxid“ bezeichnet (Oxide = Sauerstoffverbindungen). Den Oxidationsvorgang selbst nennt man Korrosion. Der Begriff stammt von dem lateinischen Verb corrodere ab und bedeutet so viel wie zernagen, zerfressen.
Das Wasser, das sich in der Luft findet, genügt, um die chemische Reaktion in Gang zu setzen. Je mehr Wasser, desto heftiger die Reaktion. In Gegenden mit hoher Luftfeuchtigkeit, wie beispielsweise in Südostasien, läuft der Oxidationsvorgang folglich schneller ab als in trockenen Gebieten wie der Sahara[1].
Zu Anfang bildet der Rost eine dünne Schicht auf der Oberfläche des Eisens, die Oxidschicht. Da Rost sehr porös (sprich, durchlässig) ist, gerät das darunterliegende Eisen in Kontakt mit Luft und Wasser und fängt ebenfalls an zu rosten, bis nach und nach das gesamte Eisenstück nur noch aus Rost besteht.
Der Rost „frisst“ sich also durch das Eisen durch. Das sieht dann nicht nur unschön aus, sondern kann auch überaus gefährlich sein, da das Eisen brüchig und spröde wird.
Eine kleine Exkursion für die Chemie-Interessierten unter uns
Wie so vieles auf der Welt ist auch die Entstehung von Rost nichts anderes als die chemische Reaktion von aufeinandertreffenden Stoffen. Mit etwas Hintergrundwissen ist das Zustandekommen dieser Reaktion schnell verstanden.
Von kleinsten Teilchen und elektrischer Ladung
Atome sind daher in ihrer Reinform elektrisch neutral. Das heißt jedoch nicht, dass Atome verschiedener Art dieselbe Anzahl an Protonen (und demnach Elektronen) aufweisen. Während man im Wasserstoffatom zum Beispiel nur ein Proton und ein Elektron vorfindet, zeigen sich im Goldatom 79 Protonen und 79 Elektronen.
Gehen nun zwei oder mehrere Atome derselben oder unterschiedlichen Art eine Bindung miteinander ein, entsteht ein Molekül. Dabei verlinken sich die Elektronen der jeweiligen Atome paarweise. Da jedoch verschiedene Atomarten unterschiedlich viele Elektronen aufweisen, geht die Rechnung nicht immer ganz auf, sodass manchmal Elektronen unverbunden bleiben.
Neben elektromagnetischen Vorgängen in der Umwelt (durch die übrigens auch reine Atome ihre elektrische Neutralität verlieren können), sorgt dies dafür, dass Moleküle nicht zwingend neutral geladen sind.
Atome und Moleküle mit elektrischer Ladung nennt man Ione. Herrscht ein Elektronenüberschuss vor, ist das Ion negativ geladen. Bei einem Mangel an Elektronen findet man eine positive Ladung vor. Negativ geladene Ionen nennt man Katione, positiv geladene Ionen Anione.
Das Streben nach dem Edelgaszustand
Nun muss man wissen, dass alle Atome und Moleküle stets einen Edelgaszustand anstreben, da er Stabilität und Reaktionsträge verleiht und somit die energetisch günstigste Form ist, die erreicht werden kann.
Sie kommt zustande, sobald sich in der äußersten Atomschale genau acht Elektronen befinden – nicht mehr, nicht weniger (das nennt man die Oktettregel).
Der Edelgaszustand wird erreicht, indem bei der Reaktion von Atomen miteinander Elektronen abgegeben bzw. aufgenommen werden. Kationen sind in aller Regel Elektronenräuber, während Anionen ihre überschüssigen Elektronen händeringend loswerden möchten.
Den Prozess der Elektronenaufnahme nennt man Oxidation. Aufgrund ihrer chemischen Beschaffenheit stoßen Metalle grundsätzlich Elektronen ab. Diese werden dann von den bei der Reaktion beteiligten Nichtmetallen aufgenommen.
Die Reaktion von Eisen mit Sauerstoff und Wasser
Auch die chemische Reaktion, die durch den Kontakt von Eisen mit Sauerstoff und Wasser ausgelöst wird und Rost entstehen lässt, findet auf molekularer Ebene statt. Dem Sauerstoffmolekül dürstet es nach Elektronen, da es nur sechs in seiner äußeren Schale hat und ihm zwei zum Erreichen des Edelgaszustandes fehlen.
Da Eisen ein Metall ist, gibt es nur zu gerne einige seiner Elektronen ab und bildet, wie andere Nichteisenmetalle auch, nach der Abgabe seiner Elektronen eine dünne Oxidschicht, um sich vor weiteren äußeren Einflüssen zu schützen. Wäre da nicht die Feuchtigkeit, die – egal, wo man sich auf der Welt befindet – immer in der Luft hängt, würde die Geschichte an dieser Stelle gut enden.
Sobald jedoch Feuchtigkeit in der Luft vorhanden ist, reagiert sie mit den Sauerstoffmolekülen, noch bevor diese isoliert mit dem Eisen oxidieren können. Dabei verbinden sich stets ein Sauerstoffmolekül mit zwei Molekülen Wasserstoff zu vier Hydroxidionen. Dieser Vorgang benötigt die Aufnahme von vier Elektronen[2]. Das Eisen, das ohne Probleme zwei Elektronen abgeben kann, kriegt nun vier entzogen und leidet unter Elektronenmangel.
Da es folglich positiv geladen ist, wird es von den negativ geladenen Hydroxidionen angezogen und verbindet sich mit diesen. Dabei entsteht zunächst grün bis olivbraun gefärbtes Eisen(II)-, und später rostbraunes Eisen(III)-Hydroxid. Rost ist chemisch gesehen also ein wasserhaltiges Eisenoxid, genauer gesagt die Verknüpfung von Eisen(II)-Oxid, Eisen(III)-Oxid und Kristallwasser.
Dadurch, dass die Eisenmoleküle die Hydroxidionen in sich aufnehmen, wächst ihre Masse, und so auch ihr Volumen. Beim Aufblähen schwindet die Festigkeit der Metallstruktur und es kommt zu Spannungen, wodurch das Gefüge brüchig wird und abplatzt.
Unter den abgeplatzten Stellen kommt reines Eisen zum Vorschein, das nun mit Sauerstoff und Wasser in Kontakt kommt. Der Oxidationsprozess wird erneut in Gang gesetzt, bis das gesamte Eisenstück Stück für Stück zerbröselt ist. Diesen langsamen Verfall nennt man Verwitterung[3].
Was passiert, wenn Eisen mit Säure oder Salzen in Kontakt kommt?
Eisen korrodiert nicht nur in Verbindung mit Sauerstoff. Auch der Kontakt mit Säure kann einen Korrosionsprozess auslösen, den man dann Wasserstoffkorrosion nennt. Wie bei der Sauerstoffkorrosion auch entziehen die positiv geladenen Wasserstoffionen der Säure dem Eisen die Elektronen.
Unter Laborbedingungen wird das Metall dabei jedoch nur spröde und instabil. Auch hier – genauso wie bei der Reaktion mit Sauerstoff – bildet sich Rost erst dann, wenn Wasser bzw. Feuchtigkeit mit ins Spiel kommt[4].
Möchte man den Korrosionsprozess, gleich mit Sauerstoff oder Säuren, beschleunigen, muss man nur dafür sorgen, dass das Eisen mit Salzen (z.B. Natriumchlorid) in Berührung kommt. Salze verstärken die elektrische Leitfähigkeit von Wasser, wodurch der Austausch von Elektronen (also der Oxidationsprozess) permanent und mit höherer Geschwindigkeit vonstatten geht.
In unserem Fall begünstigen sie die Verschmelzung von Sauerstoff und Wasser zu Hydroxidionen und deren Aufnahme von Eisenelektronen. Aus diesem Grund rosten gerade Schiffe auf Meeren und Nichtedelmetalle nahe Häfen und Salzgewässern besonders schnell[5].
Die Gefahren von Rostbildung

Egal, um welche Art von Metallobjekt es sich handelt – gleich ob Stahlträger, Werkzeug, Tischbein oder Zaunpfahl –, der Gegenstand kann seine Funktion nicht mehr erfüllen. Im besten Fall ist er für uns nutzlos geworden, im schlimmsten Fall, wenn der Rost nicht rechtzeitig entdeckt worden ist, sogar gefährlich.
Aber mehr als nur zu brechen, kann Rost auch Reibungswiderstand bilden. Dadurch, dass die Oberfläche des Metalls porös und flockig wird, verliert sie an Glätte. Besonders relevant wird diese Tatsache, wenn das Metall ein sich bewegendes Teilstück in einem Gegenstand ist und durch den Reibungswiderstand beginnt zu klemmen oder gar ganz stecken bleibt. Motoren können stehenbleiben, Schrauben und Muttern können sich verhaken.
Rostbildung hemmt darüber hinaus die elektromagnetischen Eigenschaften des Metalls. Der (teilweise) Verlust des Magnetismus ist natürlich nicht immer tragisch. Wenn wir keine Kühlschrankmagneten an Parkbänke und Bahnschienen kleben können, geht die Welt nicht unter.
Doch alleine schon bei Kochgeschirr kann schwindende magnetische Leistung bei denjenigen von uns zu Problemen führen, die mit Induktionsherden arbeiten. Wirklich Schaden tragen dann beispielsweise Automobil- und Elektronikindustrien davon, deren Funktionstüchtigkeit vom Magnetismus ihrer Geräte abhängt.
Auch Industrien im energieerzeugenden Sektor verzeichnen Ausfälle bei Rostbildung, da Rost wie ein Isolierstoff wirkt und den elektrischen Fluss stört.
Schließlich können sich in rostigen Gegenständen unter Umständen Tetanus Bakterien ansammeln. Solange man aber keine offene Wunde hat, durch welche die Bakterien in den Blutkreislauf gelangen können, muss man sich diesbezüglich keine Sorgen machen.
Da Tetanus Bakterien erdansässig sind, ist es darüber hinaus sehr unwahrscheinlich, dass sie sich in Rost finden lassen, der nicht zumindest in unmittelbarer Nähe von Erde oder mit Erde in Berührung gekommen ist.
Wie man Stahl und Eisen vor Rost schützt
Selbstverständlich gibt es zahlreiche Wege, Eisenmetalle vor Rost zu schützen. Wäre dem nicht so, würden Eisen und Stahl schon lange nicht mehr einen so häufigen und vielfältigen Einsatz im Arbeits- und Privatleben finden.
Eine der einfachsten Methoden, um einem Rostbefall entgegenzuwirken, ist ohne Frage, das Metall mit einer Beschichtung zu überziehen. Dabei kann es sich um Stoffe wie Emaille, Teflon oder Keramik handeln, aber auch um spezielle Farben und Lacke, wie sie beispielsweise bei Autos zum Einsatz kommen.
Für Stahl nimmt man häufig sogar Beton als Beschichtung, wodurch der bekannte Stahlbeton bzw. Betonstähle entstehen[6]. Eine lückenlose Beschichtung gleicht einem Schutzschild, das verhindert, dass das Metall mit Luft und Sauerstoff in Berührung kommt.
Im Falle von Stahl wirkt man der Rostbildung auch gerne durch die Zugabe von anderen Stoffen entgegen. Ab einem Anteil von zehn Prozent Chrom im Stahl darf dieser als rostfrei bezeichnet werden. Beträgt der Chromgehalt um die vierzehn Prozent, handelt es sich bereits um hervorragenden Edelstahl.
Am Ende des Tages ist jedoch der Zusatz von Chrom nichts anderes als eine Form der Beschichtung, denn er wirkt, indem er sich als dichte Passivschicht aus Chromdioxid an der Oberfläche festsetzt. Auch Niob, Mangan, Molybdän oder Nickel können Stahl als Legierungselemente zugegeben werden und wirken in der Regel sogar noch besser als Chrom. Man darf sich jedoch nicht von dem Begriff „rostfrei“ in die Irre leiten lassen.
Unter besonders aggressiven Umweltbedingungen (u.a. bei extremen Temperaturen, Feuchtegraden, pH-Werten, Chlor- oder Salzgehalten oder in Berührung mit Schwefeloxid) kann auch Edelstahl oxidieren[7].
Eine weitere Methode, Eisen vor Rost zu schützen, ist das Anbringen einer Opferanode. Eine Opferanode ist ein Stück Metall, das sich wortwörtlich für das Eisen aufopfert, indem es selbst verrostet.
Dabei muss es sich um ein unedleres Metall als Eisen handeln, sodass es früher als das Eisen mit der Korrosion beginnt. Die Opferanode muss in direkter Berührung an das Eisen angebracht sein, damit sie ihre Elektronen, die während der Korrosion freigesetzt werden, an das Eisen abgeben kann.
Das Eisen hat dadurch ständig genug neue Elektronen, wodurch der Entzug der eigenen Elektronen durch Luft und Wasser wirkungslos bleibt[8].
Zum Korrosionsschutz zählen auch Rostumwandler, die nachträglich aufgetragen – also, nachdem das Eisen bereits Rost angesetzt hat – das Eisenoxid in hartes, mattgraues Eisenphosphat umwandeln. Die mit am häufig verwendetsten Rostumwandler sind heutzutage Phosphorsäure und Phosphate[9].
Der einfachste und günstigste Trick, um rostendem Metall vorzubeugen, ist jedoch der: Man halte das Metall, sei es Eisen oder Stahl, stets so trocken wie möglich.
Rostet nur Eisen?
Eisen, bzw. Eisenverbindungen, sind tatsächlich die einzigen Metalle, die Rost ansetzen. Das heißt jedoch nicht, dass sie die einzigen Metalle sind, die mit Sauerstoff unter Einfluss von Feuchtigkeit reagieren und anschließend korrodieren.
Allerdings ist nicht jede Art von Korrosion für Metalle schädlich. Bei den meisten Metallen (den sog. Nichteisenmetallen, wie Kupfer, Aluminium, Chrom oder Zink) entsteht bei der Korrosion lediglich eine dünne, harte Mineralschicht, die das Metall wie ein Mantel umhüllt – die Oxidschicht. Im Gegensatz zu Rost ist sie undurchlässig und schützt das darunterliegende Metall vor weiteren äußeren Einflüssen[10]. Ein Beispiel für eine solche Schutzschicht (die übrigens Patina genannt wird) findet man oft an Denkmäler in älteren Städten.
Die aufgesetzten Verblendungen aus Kupfer färben sich mit der Zeit grün, wie bspw. die Kuppeln des Berliner Doms und des Wasserturms in Mannheim (und das Dach des gegenüberliegenden Rosengartens), die Dächer des Hamburger und Bremer Rathauses und das Gewölbe am Dresdner Zwinger. Auch die Freiheitsstatue mit ihrer blau-grünen Färbung war einst kupferbraun.
Der Farbton der Patina und seine Schattierung können je nach Metall und Standort stark voneinander abweichen, da sie von der chemischen Zusammensetzung des Metalls und den vorherrschenden Wettergegebenheiten abhängen.
…und wie war das jetzt noch einmal mit Rost und dem gusseisernen Kochgeschirr von ROETH No1?
Nach allem, was wir nun über die Voraussetzungen für die Entstehung von Rost wissen, ist klar, dass Gusseisen grundsätzlich rosten kann, und unter den richtigen Bedingungen auch rosten wird. Selbst dann, wenn es zu Kochgeschirr verarbeitet worden ist. Ganz wichtig ist an dieser Stelle aber zu erwähnen – und wir können es gar nicht oft genug sagen –, dass das nur für unbeschichtetes Kochgeschirr gilt!
Unbeschichtetes Kochgeschirr aus Gusseisen kann rosten
Das Einbrennen einer Patina hilft kaum gegen die Rostbildung bei unbeschichtetem Kochgeschirr. Denn zum einen bilden sich relativ leicht winzige Risse in der Patina, egal, wie achtsam man bei der Reinigung ist. Schließlich handelt es sich bei der Patina um nichts anderes als eingebranntes Fett, dass zwar für einen Antihaft-Effekt sorgt, jedoch bereits durch einen Holzschaber Risse bekommen kann, weswegen sie auch regelmäßig erneuert werden muss.
Durch die Risse in der Patina gelangen Luft und Feuchtigkeit an das Eisen.
Zum anderen überzieht die Patina nur den Innenboden der Pfanne; Ränder und Unterboden bleiben unbedeckt und bieten eine wunderbare Angriffsfläche für Sauerstoff und Nässe.
Natürlich ist anzumerken, dass gusseisernes Kochgeschirr höchstens im Sommer zum Grillen ein paar Mal, und dann auch nur für einen beschränkten Zeitraum, im Freien ist. Gelagert wird es in aller Regel irgendwo im Haus, wo die Luftfeuchtigkeit normalerweise geringer ist als draußen.
Da das Gussgeschirr weder Regen noch Nebel oder Schnee jemals ausgesetzt ist, beginnt der Korrosionsprozess wesentlich später als bei anderen Gegenständen und geht auch sehr viel langsamer vonstatten. Oft kann es mehrere Jahre dauern, bis sich der erste Rostfleck zeigt.
Wichtig ist einfach immer, unbeschichtetes Kochgeschirr gründlich abzutrocknen, bevor man es zurück in den Schrank stellt, um so eine feuchte Lagerung zu vermeiden und dem Rost keine Handreichung zu leisten.
Beschichtungen schützen vor Rost
Beschichtete Töpfe und Pfannen aus Gusseisen sind in aller Regel äußerst gut vor Rostbildung geschützt. Ist die Oberflächenbeschichtung rundum intakt, muss man sich keine Sorgen machen. Dabei ist es ganz egal, ob die Beschichtung aus Emaille oder Teflon besteht.
Wichtig ist nur, dass sie den gesamten Pfannenkörper umzieht und keine tiefen Kratzer aufweist. Klar. Denn sobald die Möglichkeit besteht, dass Luft und Feuchtigkeit an das Gusseisen gelangen, besteht auch die Möglichkeit von Rost.
Solange man das Kochgeschirr nicht benutzt, ist es also egal, ob es sich bei der Oberflächenbeschichtung um Emaille oder Teflon handelt. Kommt es aber zum Einsatz (wie es bei Kochgeschirr so sein sollte), kristallisiert sich schnell heraus, dass Emaille die praktischere Lösung ist.
Emaille hat eine glasartige, harte Oberfläche, die extrem widerstandsfähig gegenüber Kratzer ist[11]. Um einen Kratzer in Emaille zu bekommen, muss man sich sehr anstrengen – mehr noch, um ihn so tief zu machen, dass er einen Weg zum darunterliegenden Eisen freigibt.
Teflon hingegen ist ein weicher Stoff, bei dem man sehr Acht geben muss, ihn nicht zu beschädigen. Darüber hinaus flockt er ab einer gewissen Anzahl an Nutzungen langsam aber stetig von alleine ab.
Wie man Rost von einer unbeschichteten Gusspfanne entfernt
Selbst, wenn man seine Pfanne nach dem Abwaschen immer so gründlich wie möglich abtrocknet, kann es irgendwann trotzdem einmal passieren, dass sie Rost ansetzt. Das ist zwar wirklich ärgerlich, aber alles andere als ein Weltuntergang.
Seit es Eisen gibt, gibt es auch Rost, und vermutlich beinahe eben so lange auch Mittel, diesen zu entfernen. Zur Auswahl gehören harte Bürsten und Sandstrahlmaschinen, chemische Lösungen und Essig, Zitronensäure und Natron.
Wie bei allem zählt auch bei der Entfernung von Rost an Pfannen: Je früher das Problem entdeckt wird, desto leichter kann man es auflösen. Das Wenige, was es zur Rostentfernung benötigt, findet man sogar meist in der eigenen Küche. Dank unserer folgenden zwei simplen Methoden strahlt die Pfanne im Nu wie neu.
Die Kartoffel-Salz-Methode
Die Kartoffel-Salz-Methode[12] ist eine super einfache Methode, die Rostflecken auf der Eisenpfanne verschwinden zu lassen. Leider verursacht sie etwas Dreck und Unordnung, aber man kann im Leben nicht alles haben… oder doch?
Legt man die Arbeitsfläche vor Beginn mit alten Zeitungen aus oder erledigt den Job bei gutem Wetter einfach gleich im Freien, wird die Küche beinahe gar nicht schmutzig. Alles, was man dann noch braucht, ist grobkörniges Salz, Pflanzenöl und eine Kartoffel. Und so geht‘s:
- Zuerst eine ordentliche Portion Salz in die Pfanne streuen. Zur Orientierung – bei einer Pfanne mit einem Durchmesser von ca. 30 cm kann man mit einer guten Handvoll Salz (circa 100 g) beginnen.
- Dann die Kartoffel so schneiden, dass eine der beiden Hälften angenehm und fest in der Hand liegt.
- Mit der aufgeschnittenen Kartoffelseite das Salz kraftvoll auf der Pfanne einreiben.
- Die Feuchtigkeit der Kartoffel sorgt dafür, dass sich der Rost vom Eisen lösen kann. Für das schönste Ergebnis sollte man sich mit ordentlichem Druck in kreisartigen Bewegungen von innen nach außen vorarbeiten. Hat die Pfanne Grillrippen, fährt man am besten an diesen entlang. Boden, Griff, Stiel und Seiten nicht vergessen.
- Je nachdem, wie rostig die Pfanne am Anfang ist, kann es ratsam sein, das inzwischen schlammig braun gewordene Salz durch Neues zu ersetzen.
Das geht am einfachsten, indem man die Pfanne schnell ausspült, abreibt und neues Salz draufstreut. - Sind alle Rostflecken entfernt, die Pfanne gut mit Wasser ausspülen und ordentlich trocken wischen.
Anschließend am besten im Backofen auf niedriger Temperatur ungefähr eine Minute lang erhitzen. So stellt man sicher, dass absolut keine Feuchtigkeit mehr an der Pfanne haftet. - Ist die Pfanne durch und durch trocken, mit einer kleinen Menge Öl einreiben und noch einmal für eine halbe Stunde auf dem Herd erwärmen.
Dadurch wird eine neue Schutzschicht eingebrannt, welche erneutes Rosten erschwert. - Tada! Schon glänzt die Pfanne wie funkelnagelneu. Um sie so gut wie möglich vor neuem Rost zu schützen, sollte man sie in einem trockenen Schrank aufbewahren und – das ist das Wichtigste – so oft wie möglich benutzen.
Die Essig-Einweich-Methode
Die Essig-Einweich-Methode[13] ist für die Pfannenliebhaber unter uns geeignet, denen das Einbrennen der Pfanne wenig ausmacht.
Um den Rost loszuwerden, braucht man Essig Essenz, mildes Spülmittel, einen Schwamm viel Wasser und Öl, um die zerstörte Patina am Ende wieder einzubrennen.
- Zuerst Essig und Wasser in gleicher Menge in einem Behälter mischen. Der Behälter muss so groß sein, dass die Pfanne ganz darin versinken kann. Bevor man sich aber verrückt macht – das Spülbecken tut es auch. Doch Vorsicht bei hellen Spülen – der Rost kann auch dort beim Ablösen Schmiere hinterlassen! Wie lange die Pfanne in der Essig-Wasser-Mischung einweichen muss, hängt davon ab, wie viel Rost sich angesammelt hat. Das kann im ärgsten Fall bis zu acht Stunden bedeuten. Wenn man seine Pfanne gerne mag (und das tun wir), sollte man immer mal wieder ein Auge auf das Ganze werfen. Denn…
- …sobald sich die Rostflecken wie von selbst von der Pfanne lösen, muss sie aus dem Wasser genommen werden. Der Essig hat nicht nur auf Rost eine zerstörende Wirkung, sondern fängt kurz danach auch an, das Eisen selbst anzugreifen ⁴.
- Der kleine Nachteil bei der Essig-Einweich-Methode ist, dass die Essigmischung auch die Patina von der Pfanne ablöst. Das Malheur ist aber schnell behoben. Nachdem man den ganzen Rost von der Pfanne geschrubbt hat, wäscht man sie mit Schwamm, Spülmittel und warmem Wasser ab, sodass sie am Ende frei von Essig ist. Danach zum Trocken kurz in den Backofen stellen oder mit einem Tuch abreiben.
- Nun kann man mit dem erneuten Einbrennen beginnen. Die Pfanne vom Boden bis zum Stiel mit Pflanzenöl einreiben und eine Stunde lang auf höchster Stufe in den Backofen stellen. Man sollte unbedingt daran denken, einen Auffangbehälter auf das Blech darunter zu stellen, da sich beim Erhitzen kleine Fetttröpfchen von der Pfanne lösen können. Danach die Pfanne abkühlen lassen. Um Rostflecken vorzubeugen, kann man seine Pfanne nach jedem Gebrauch mit einer Schicht Öl einreiben. Dadurch bildet sich nicht nur eine effektive Schutzwand, es bildet sich außerdem eine glattere Oberfläche – Win-win.
- Die Pfanne sollte immer in einem trockenen Platz mit wenig Luftfeuchtigkeit aufbewahrt werden. Man kann Eisenpfannen sogar stapeln. Alles, was man dazu tun muss, ist eine Serviette oder ein Papierhandtuch zwischen die einzelnen Gusspfannen legen.
Exkurs: Wenn unbeschichtete gusseiserne Pfannen rauchen
Zugegeben: Bis auf die Tatsache, dass beides mit einem R beginnt, hat Rauch nicht viel mit Rost zu tun. Doch da wir uns gerade mit zwei Reinigungsmethoden für unbeschichtete Pfannen beschäftigt haben, macht es Sinn, an dieser Stelle kurz auf das Problem von Rauch hinzuweisen.
Bei alten Gusspfannen ohne Beschichtung kann es durchaus vorkommen, dass sich bei der Nutzung starker Rauch bildet. In diesem Fall sollte man sich zuerst an der Kartoffel-Salz- oder Essig-Einweich-Methode versuchen, bevor man zu härteren Mitteln greift.
Bringen beide Methoden tatsächlich nichts, kann man sich überlegen, die Pfanne sandstrahlen zu lassen. Viele Industriebetriebe, die mit Metallen arbeiten, besitzen die Möglichkeit mit Sand zu strahlen. Die Oberfläche der gusseisernen Pfanne wird so definitiv blank und kann anschließend neu eingebrannt werden.
Natürlich hat nicht jeder von uns die Möglichkeit, bei einem Industriebetrieb anzufragen. Wie für alles im Leben gibt es auch hier Do-It-Yourself Heimmethoden.
Für die erste DIY-Methode braucht man ein Feuer im Freien (also zum Beispiel einen Grill) und eine Stahlbürste. Sobald die Pfanne heiß ist, schrubbt man sie hart mit der Stahlbürste ab. Dieses Vorgehen benötigt viel Kraft – und viel Vorsicht, denn es ist erschreckend einfach, sich dabei zu verbrennen.
Für die zweite Heimmethode braucht man Backofenspray (am besten mit Bio-Siegel) und ein Tuch. Nachdem die Pfanne ordentlich eingesprüht ist, lässt man das Mittel 24 Stunden lang einwirken. Dann wischt man es gründlich ab und wiederholt den Vorgang.
Sowohl bei der Stahlbürsten- als auch der Backofenspray-Methode darf man nicht vergessen, die Pfanne danach wieder ordnungsgemäß einzubrennen.
Eisen rostet, Emaille nicht

Allen, die ihre Gusspfanne von Oma ohne Beschichtung geerbt haben, sollten unsere zwei Entroster-Heimmethoden das Leben erleichtern.
Viel Spaß beim Grillen und Kochen in der rostfreien, glänzenden Gusspfanne wünscht
das Roeth No1 Team
[2] https://www.schule-studium.de/Chemie/Chemieunterricht/Reaktionsgleichung-Rosten-von-Eisen.html
[3] https://www.chemie-schule.de/KnowHow/Rost
[4] https://www.chemie-schule.de/KnowHow/Rost
[5] https://www.theo-schrauben.de/blog/wie-entsteht-rost/
[6] https://wissen.lauftext.de/die-natur/chemie/warum-rostet-eisen_.html
[7] https://www.rostfrei-stahl.com/blog/detail/das-geheimnis-von-rostfreiem-stahl/
[8] https://www.theo-schrauben.de/blog/opferanode/
[9] https://www.chemie-schule.de/KnowHow/Rost
[10] https://www.reliance-foundry.com/blog/stages-of-rust
[11] http://www.fachwissen-technik.de/verfahren/emaillieren.html
[12] http://www.apartmenttherapy.com/how-to-clean-and-season-old-ru-151535
[13] http://www.bonappetit.com/test-kitchen/how-to/article/cast-iron-pan-rust

Mehr als danke dafür. Wirklich profunde Anleitungen.
Mit freundlichen Grüßen,
Radulph
Hallo Christian,
deine Tipps sind ja eher für die schlimmen fälle, wie bekomme ich den einzelne Rostpunkte am effektivsten weg?
Grüße Andreas
Hallo Christian,
also die Kartoffelmethode kannte ich bisher nur vom Einbrennen. Aber man
lernt eben nie aus!
Hallo, habe mir vor einigen Jahren eine geschmiedete unbeschichtete Pfanne gekauft, da ich mit den beschichteten schlechte Erfahrungen gemacht habe.
1. die Pfanne wie beschrieben einbrennen, dann
2. ich benutze diese Pfanne nur zum heiß braten von Fleisch und Wurst, brennt bei mir nichts an,
3. wenn sich bei panierten Schnitzeln mal was ansetzt, dann mit Stahlschwamm reinigen,
4. nach Gebrauch Pfanne noch warm mit genügend Küchenpapier sauber ausreiben und nicht auswaschen, Pfanne bleibt trotzdem hygienisch sauber
5. danach Pfanne mit etwas Öl einfetten und bis zum nächsten Gebrauch in Küche wegstellen, nicht in nassen Räumen aufbewahren!